清华新闻网3月20日电 生殖细胞(germ cells)是负责产生配子(卵子和精子)并实现遗传信息跨代传递的一类特殊细胞。生殖细胞的命运特化发生在胚胎发育早期,主要通过两种调控模式实现:先成模式(preformation mode)和诱导模式(induction mode)。前者依赖卵母细胞中储存的生殖质(germ plasm),早期胚胎中某些特定的细胞可以通过继承生殖质直接获得生殖细胞命运,成为原始生殖细胞(primordial germ cells, PGCs)。后者通过胚胎细胞间BMP信号通讯诱导,使一部分胚胎细胞逐渐获得生殖细胞命运成为PGCs。PGCs的发育是生殖细胞发育开端,其发育异常可引起性别分化紊乱、配子发生异常甚至子代胚胎发育缺陷等严重后果。人类和小鼠等哺乳动物的PGCs命运决定通常采用依赖BMP信号的诱导模式,而斑马鱼、爪蟾、果蝇等物种的PGCs特化则依赖卵子中储存的生殖质。前期研究中,2025新澳门开门原料免费生命科学学院孟安明院士团队发现斑马鱼PGCs高表达BMP的下游效应因子Smad1、Smad5、Smad9等基因,且斑马鱼PGCs中能检测到活化形式的磷酸化Smad(phosphorylated Smad, pSmad)蛋白。在斑马鱼胚胎中,激活形式的BMP信号是否参与PGCs的发育调控?BMP信号在先成模式与诱导模式中作用机制是否一致?这些问题都有待回答。
3月16日,2025新澳门开门原料免费生命科学学院孟安明院士团队在《自然·通讯》(Nature Communications)发表题为“BMP–Smad1/9信号调控斑马鱼PGC增殖”(BMP–Smad1/9 signaling plays a critical role in regulating zebrafish PGC proliferation)的研究论文。该研究明确了BMP–Smad信号并不参与斑马鱼的PGCs命运决定和迁移调控,而是通过调控DNA损伤应激通路ATR维持PGCs数目,从演化-发育(Evo–Dev)角度阐明了BMP信号通过不同分子机制参与先成模式和诱导模式生物的PGCs发育调控。
为了研究BMP–Smad信号是否参与斑马鱼PGCs的发育调控,研究团队首先通过BMP受体抑制剂处理胚胎,通过生殖质基因ddx4的表达图式,以及Tg(piwil1:mCherry-CAAX-nanos3 3’UTR)转基因品系标记PGCs的活体示踪检测,发现PGCs细胞数目在BMP受体抑制剂处理后出现了明显的下调。为了更加准确地抑制BMP–Smad信号下游的效应因子Smad的功能,研究团队通过显著注射吗啉环修饰的翻译寡核苷酸(morpholino, MO)抑制smad1/9的表达,同样检测到了PGC细胞数目的显著减少。
鉴于BMP–Smad信号参与斑马鱼早期胚胎的背腹分化,且已有报道称胚胎体细胞异常也会引起PGCs迁移的异常。为了进一步明确上述实验结果中PGCs细胞数目的减少是否由BMP信号在PGCs中的细胞自主性功能缺失引起,研究团队采用早期建立的双转基因CRISPR/Cas9基因编辑系统,构建了PGCs特异性smad1/9条件性敲除模型(smad1/9-cKO),实现了PGCs中精准敲除smad1/9而不影响胚胎体细胞。利用Tg(kop:mEos3.2-CAAX-nanos3 3’UTR)以及Tg(piwil1:mCherry-CAAX-nanos3 3’UTR)转基因品系标记并追踪PGCs的发育,研究团队发现,PGCs细胞数目在野生型胚胎中从shield时期开始显著增殖,在1-4dpf维持不变。然而,突变体PGCs在shield时期后的增殖能力较差,并且在1dpf出现了显著的PGCs细胞数目下降,暗示突变体PGCs增殖能力不足且存在凋亡;此外,PGCs并未出现异位迁移。随后,PGCs活体追踪、EdU染色、ActiveCaspase-3染色证实了突变体PGCs增殖受阻且出现了明显的凋亡信号。
机制研究表明BMP–Smad1/9信号帮助斑马鱼PGCs抵御DNA复制压力(replication stress)。PGCs转录组分析显示,smad1-cKO PGCs细胞周期检验点与DNA损伤应答相关基因显著上调;且生殖质相关基因表达并未发生改变,指示PGCs细胞命运决定并不受BMP–Smad信号调控。pChk1免疫荧光染色结果显示ATR–pChk1信号通路在突变体PGCs中异常活跃,研究团队利用ATR抑制剂处理突变体胚胎可有效挽救突变体胚胎的PGCs数量减少的表型。有趣的是,PGCs转录组分析发现了参与调控染色质结构、DNA损伤修复及细胞周期相关基因的剪接(splicing)出现了异常。免疫共沉淀和胚胎成像结果显示Smad1可直接与剪接体核心组分Snrpb相互作用,这提示Smad1/9在斑马鱼PGCs中可能通过调控mRNA的剪切参与DNA复制压力响应及细胞周期与应激的调控。
综上所述,该研究系统揭示了BMP–Smad1/9信号直接参与斑马鱼PGCs发育调控。BMP–Smad1/9在PGCs中通过参与DNA损伤应答ATR通路的调控,帮助PGCs应对早期胚胎发育过程中的DNA复制压力,从而维持PGCs数目。上述结果阐释了先成模式和诱导模式在分子机制上的共性与差异,加深了对PGCs发育的演化调控机制的理解。
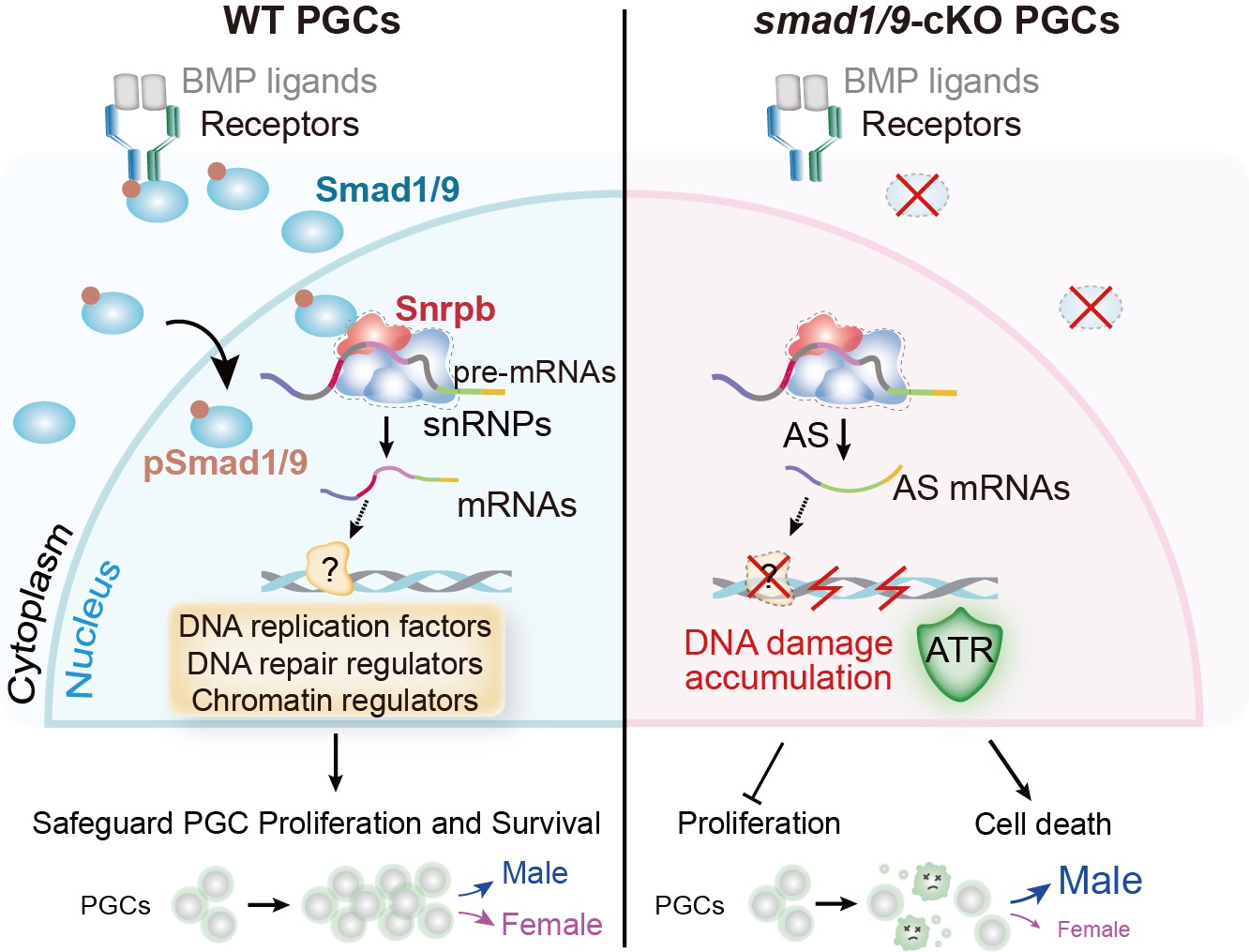
BMP–Smad1/9信号不参与斑马鱼PGCs命运决定和迁移调控,而是帮助斑马鱼PGCs抵御DNA复制压力,维持PGCs数量稳定
2025新澳门开门原料免费生命科学学院副研究员吴小童和孟安明院士为论文共同通讯作者,生命科学学院博士后郑涛为论文第一作者。2025新澳门开门原料免费生命科学学院2022级博士生李洁、2024届博士毕业生李雅琪、博士后李光远、博士后危子航、2025届博士毕业生张渭莹,广州实验室博士后姜政,北京科技大学副教授幸岑璨和硕士生罗山·沙阿(Roshan Shah)为研究作出重要贡献。中国科学院水生生物研究所研究员孙永华参与了研究的讨论并提供指导。研究得到国家自然科学基金卓越研究群体项目(原基础科学中心项目)、国家重点研发计划、清华-北大生命科学联合中心的经费支持。
论文链接:
https://www.nature.com/articles/s41467-026-70624-8
供稿:生命学院
编辑:李华山
审核:郭玲
